How Does Water Dissolve Mineral Salts?
تُعرف الأملاح المعدنية المهمة لصنع القهوة بالمركبات الأيونية، وهي متماسكة مع بعضها بروابط أيونية. وتبدأ هذه الأملاح في الذوبان . الذوبان بمجرد ملامستها للماء. وعندما يحدث هذا الذوبان، تتفكك . الأيونات التي اتحدت مع بعضها على هيئة أملاح أو تنفصل. وهذا يعني أن الأيونات المكونة للأملاح المعدنية تصبح حينها حرة في الماء ولم تعد مرتبطة ببعضها البعض. ويحدث هذا لجميع الأملاح المعدنية عندما تذوب .
لا يعتبر الماء أيونيًا، ولكنه يشبه الأيونات إلى حدٍ ما. وبسبب كون جزيء الماء قطبيًا،, فإن الشحنات الموجبة والسالبة الطفيفة على طرفيه تكفي لجذب أيون إذا عمل عدد كافٍ من جزيئات الماء معًا على ذلك. ويحيط عدد من جزيئات الماء بأيون معين، كما هو موضح أدناه، وتُبعده عن الأيونات الأخرى.
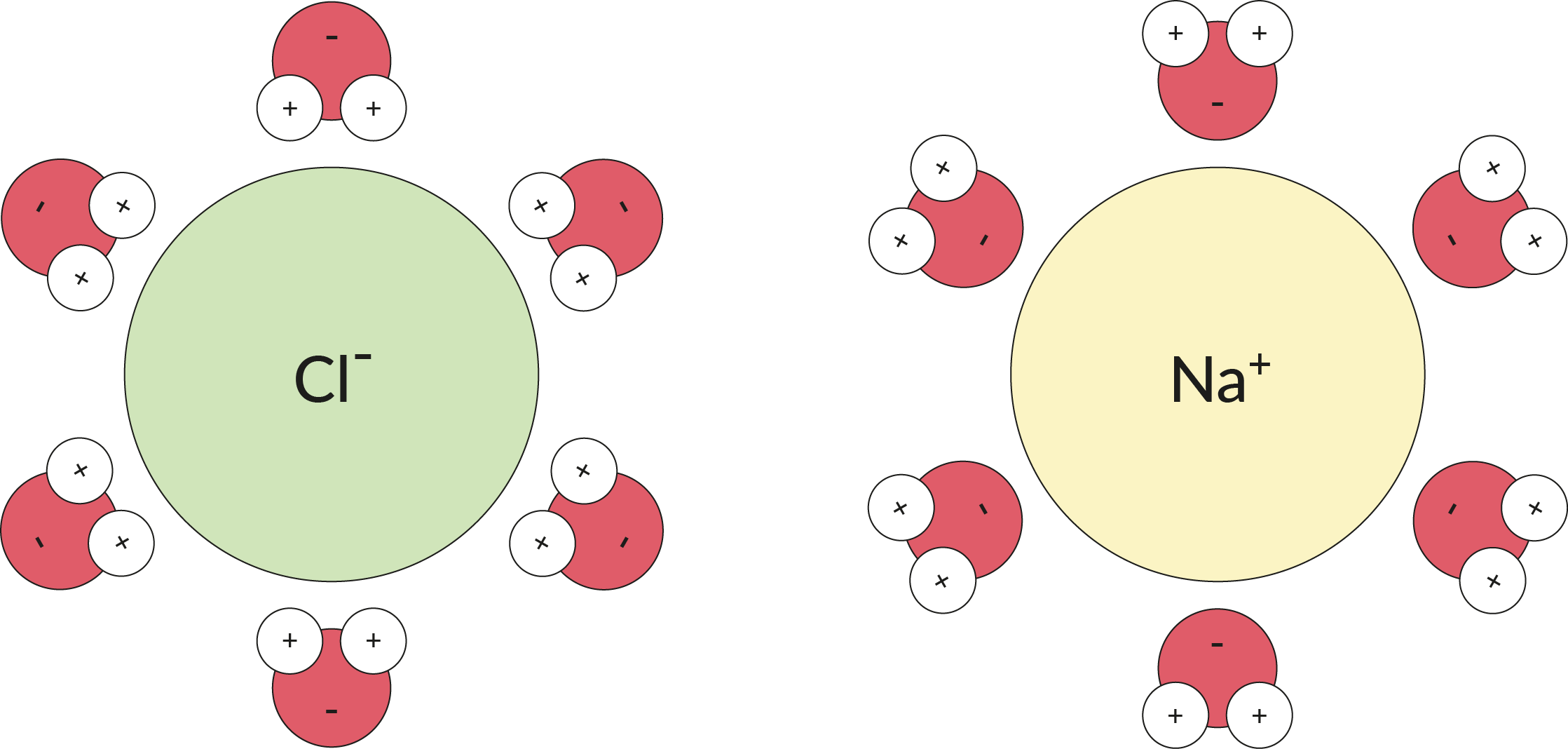
ويمكنك أن ترى في هذه الصورة كيف يتفكك ملح الطعام (NaCl)، إلى أنيون الكلوريد وكاتيون الصوديوم بعد أن تحيط ₂O جزيئات .الماء (H₂O) بكل أيون.
سرقة الإلكترونات - الروابط الأيونية
تكون جميع المعادن المهمة لصنع القهوة في شكل أملاح معدنية. وترتبط هذه الأملاح المعدنية ببعضها البعض بواسطة الترابط الأيوني فبدلاً من مشاركة إلكترون مع ذرة أخرى، تسرق الذرة إلكترونًا واحدًا أو أكثر من ذرة أخرى. ويسمى هذا النوع من الاتحاد بالرابطة الأيونية
For example, chlorine (Cl), which is used to disinfect water, has seven electrons in its outer shell. In order to become stable, it needs to ‘steal’ an electron from another atom. When it does this, it becomes negatively charged because electrons are negatively charged.
Atoms that have become charged are known as ions. The atom that steals an electron gains a negative charge and is called an anion.