Como funciona a água Dissolver Sais minerais?
Os sais minerais importantes para fazer café são conhecidos como compostos iônicos e são mantidos juntos por ligações iônicas. Assim que esses sais entram em contato com a água, eles começam a se dissolver . À medida que esta dissolução acontece, os íons que estavam ligados como um sal se separam ou se dissociam . Isto significa que os íons que compunham os sais minerais estão agora livres na água e não mais ligados uns aos outros. Isto acontece com todos os sais minerais quando eles se dissolvem .
A água não é um íon, mas age um pouco como um. Como a água é uma molécula polar , a ligeira carga negativa e positiva em cada extremidade da molécula é suficiente para atrair um íon se houver muitas moléculas de água disponíveis para trabalharem juntas. Múltiplas moléculas de água podem envolver um íon, conforme ilustrado abaixo, e mantê-lo separado de outros íons.
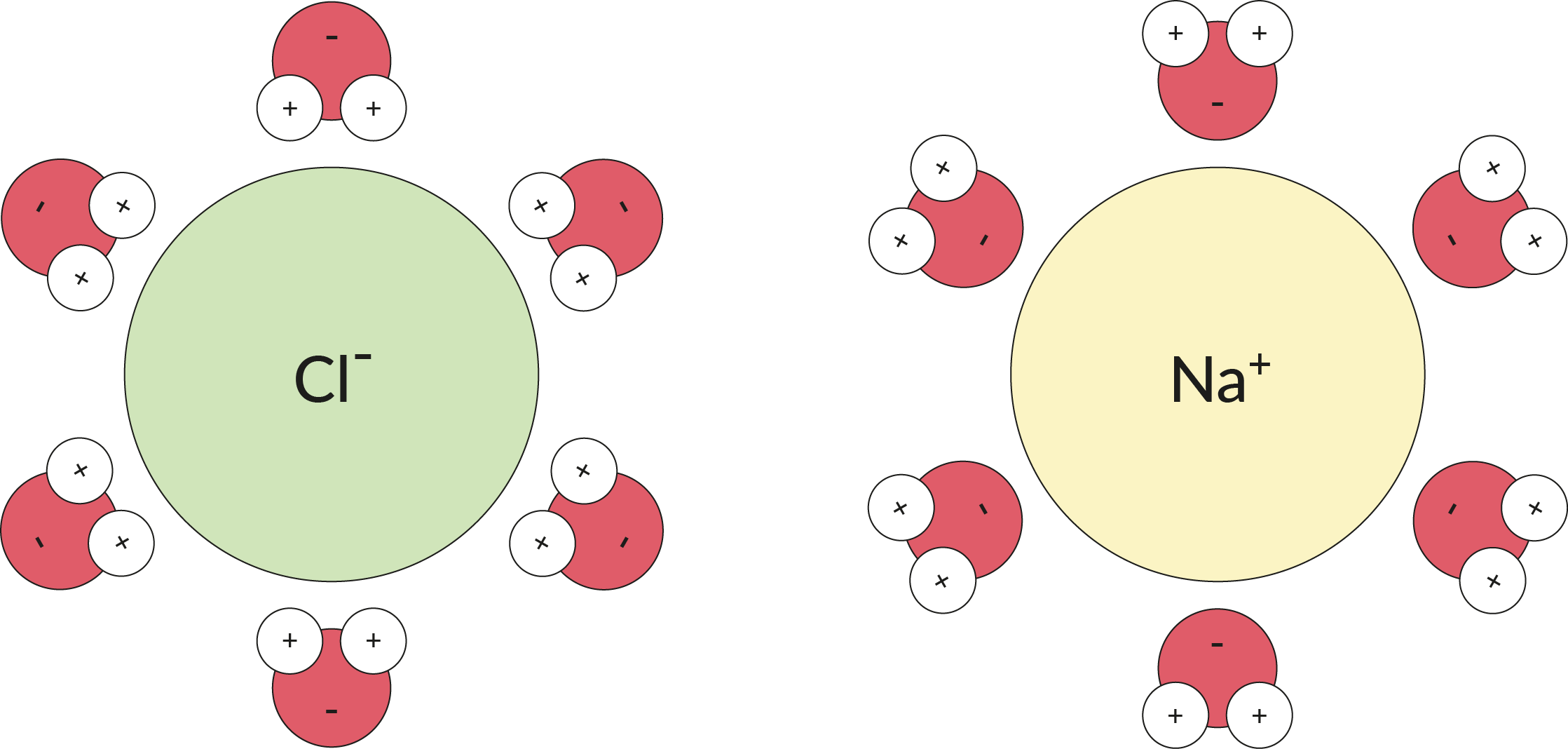
Nesta imagem você pode ver como o sal de cozinha, NaCl, pode se dissociar no ânion cloreto e no cátion sódio depois que cada íon é cercado por moléculas de H₂ O.
Roubando Elétrons – Ligações Iônicas
Todos os minerais importantes para o café assumem a forma de sais minerais. Os sais minerais mantêm-se unidos através de ligações iônicas . Em vez de compartilhar um elétron com outro átomo, um átomo rouba um ou mais elétrons de outro. Este tipo de ligação é chamada de ligação iônica , e os sais minerais são, portanto, conhecidos como compostos iônicos.
Por exemplo, o cloro (Cl), usado para desinfetar a água, possui sete elétrons em sua camada externa. Para se tornar estável, ele precisa “roubar” um elétron de outro átomo. Quando faz isso, ele fica com carga negativa porque os elétrons têm carga negativa.
Os átomos que ficaram carregados são conhecidos como íons. O átomo que rouba um elétron ganha carga negativa e é chamado de ânion.